
Die chronische spontane Urtikaria (csU) ist eine entzündliche Hauterkrankung mit hohem Leidensdruck für die Betroffenen. Dieser Beitrag gibt einen Überblick zu Symptomen, Diagnostik und Therapieoptionen. Letztere haben sich durch neue Zulassungen erheblich erweitert.
Die csU ist durch das wiederkehrende Auftreten von juckenden Quaddeln, Angioödemen oder einer Kombination beider Manifestationen über einen Zeitraum von mehr als 6 Wochen definiert [1]. Die Symptome treten plötzlich und ohne eindeutig identifizierbaren externen Auslöser auf. Die Effloreszenzen sind meist flüchtig, können jedoch über Monate bis Jahre rezidivieren und erheblich zur Krankheitslast beitragen [2].
Die weltweite Prävalenz wird auf 0,5–1,0 % geschätzt, mit regionalen Schwankungen. In Deutschland sind rund 370 000 Menschen betroffen [3]. Die Erkrankung tritt überwiegend im erwerbsfähigen Alter zwischen 20 und 40 Jahren auf und betrifft Frauen etwa doppelt so häufig wie Männer [3,4]. Bis zu zwei Drittel der Erkrankten entwickeln im Krankheitsverlauf zusätzlich Angioödeme, bei einem kleineren Anteil treten Angioödeme auch isoliert auf [5].
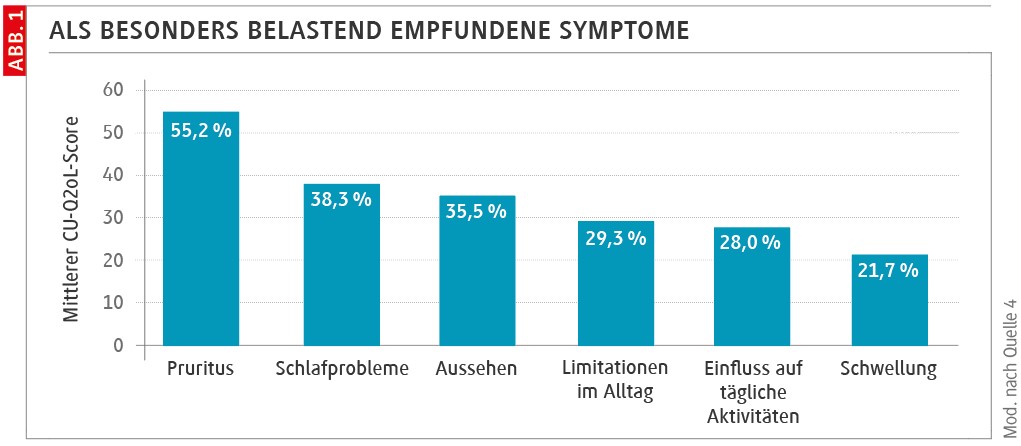
Die csU zählt zu den dermatologischen Erkrankungen mit der höchsten Krankheitslast. Neben dem oft ausgeprägten Pruritus berichten Betroffene über Schlafstörungen, Fatigue, Konzentrationsprobleme sowie eine deutliche Einschränkung der Lebensqualität (Abb. 1) [4,6]. Studien zeigen eine erhöhte Prävalenz von psychischen und somatischen Komorbiditäten [7,8].
Pathophysiologie: Mastzellaktivierung und Autoimmunität
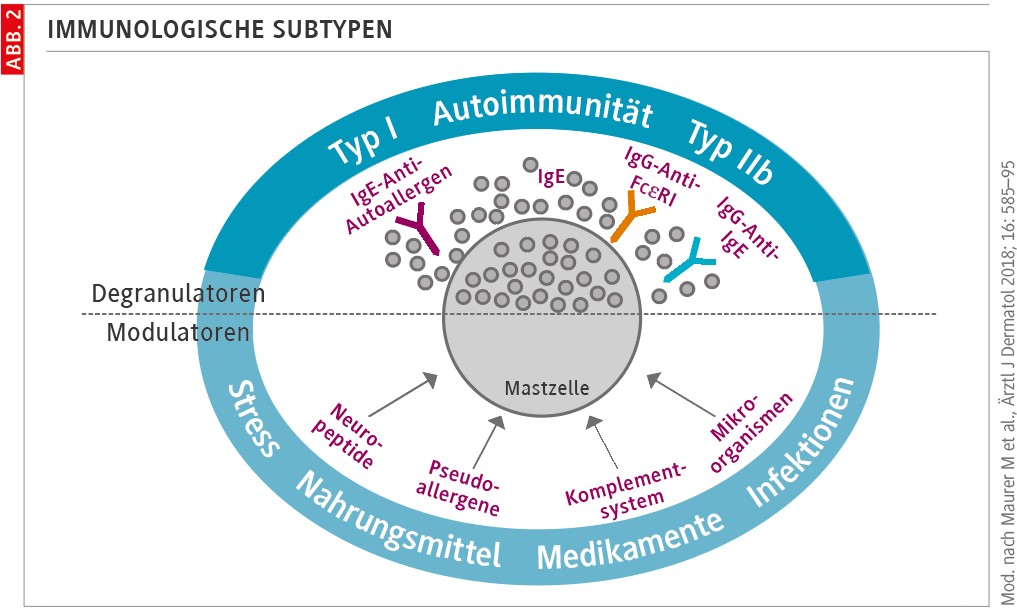
Die csU wird überwiegend als autoimmun vermittelte Erkrankung verstanden. Zentral ist die Aktivierung kutaner Mastzellen und basophiler Granulozyten mit Freisetzung von Histamin, Leukotrienen, Zytokinen und weiteren Mediatoren. Dabei lassen sich 2 immunologische Subtypen unterscheiden (Abb. 2) [9]:
Marker, die in der Praxis als Hinweis dienen können, sind u. a. niedrige Gesamt-IgE-Spiegel, Basopenie/Eosinopenie, positive funktionelle Tests (z. B. BAT), erhöhte Entzündungsparameter oder D-Dimer (nicht spezifisch) – immer im klinischen Kontext. Unabhängig vom zugrunde liegenden Autoimmunmechanismus spielt die Typ-2-Inflammation eine zentrale Rolle. Die Zytokine Interleukin-4 (IL-4) und Interleukin-13 (IL-13) fördern die IgE-Synthese, modulieren die Mastzellaktivierung und verstärken entzündliche Prozesse [10].
Diagnostik: So wenig wie möglich
Die internationale Leitlinie empfiehlt bei Verdacht auf eine csU eine zielgerichtete, schlanke Basisdiagnostik [1]. Zentraler Bestandteil ist eine strukturierte Anamnese mit Fokus auf Krankheitsdauer, Frequenz und Morphologie der Hautveränderungen, das Vorliegen von Angioödemen und potenziellen Triggerfaktoren (z. B. NSAID-Exposition, Infekte, Stress, physikalische Reize). Darüber hinaus sollte eine Medikamentenanamnese sowie eine Erhebung von Begleiterkrankungen (v. a. autoimmune) erfolgen [1].
Für die Verlaufskontrolle und Therapiestratifizierung ist die standardisierte Erfassung der Krankheitsaktivität und -kontrolle essenziell. Hierzu gehören der Urticaria Activity Score über 7 Tage (UAS7) zur Aktivitätsmessung sowie der Urticaria Control Test (UCT) zur Beurteilung der Krankheitskontrolle. Ergänzend können krankheitsspezifische Lebensqualitätsinstrumente wie der CU-Q2oL eingesetzt werden. Diese Instrumente sind notwendig, um eine unkontrollierte Erkrankung objektivierbar zu definieren und eine leitliniengerechte Therapieeskalation zu rechtfertigen [1,2].
Therapieoptionen nach Leitlinie
Die Therapie der csU folgt einem evidenzbasierten Stufenschema mit dem Ziel der vollständigen Krankheitskontrolle. Leitlinien empfehlen ein stufenweises Vorgehen beginnend mit nicht sedierenden H1-Antihistaminika, ggf. in erhöhter Dosierung [1]. Dennoch bleibt die Erkrankung bei einem relevanten Anteil der Patienten und Patientinnen unzureichend kontrolliert. Versorgungsstudien aus Deutschland zeigen, dass Leitlinienempfehlungen häufig nicht konsequent umgesetzt werden und Erkrankte entweder inadäquat behandelt werden oder trotz Behandlung über längere Zeit symptomatisch bleiben [3,6].
In der Erstlinie werden nicht sedierende H1-Antihistaminika (nsH1-AH) in Standarddosierung eingesetzt. Bei unzureichender Kontrolle ist gemäß Leitlinie eine Aufdosierung bis zum Vierfachen der zugelassenen Dosis empfohlen, wobei es sich je nach Präparat um einen Off-Label-Einsatz handelt. Hierbei ist eine individuelle Nutzen-Risiko-Abwägung erforderlich, insbesondere im Hinblick auf mögliche sedierende Effekte [1].
Persistieren die Symptome trotz hochdosierter Antihistaminikatherapie, ist Omalizumab als Add-on-Therapie der empfohlene nächste Eskalationsschritt. Der monoklonale Anti-IgE-Antikörper reduziert die Konzentration von freiem IgE und führt sekundär zu einer Downregulation des hochaffinen IgE-Rezeptors FcεRI auf Mastzellen und Basophilen, wodurch deren Reaktivität deutlich vermindert wird. Klinisch resultieren signifikante Verbesserungen von Krankheitsaktivität, Juckreiz, Angioödemhäufigkeit und Lebensqualität. Ein Nichtansprechen wird jedoch bei einem Teil der Patientinnen und Patienten beobachtet und ist endotypisch mitgeprägt [1,11].
Bei Versagen oder unzureichendem Ansprechen auf Omalizumab empfiehlt die Leitlinie Ciclosporin A als Add-on-Therapie. Der immunsupprimierend wirkende Calcineurin-Inhibitor erfordert eine engmaschige Kontrolle von Blutdruck, Nierenfunktion und potenziellen Arzneimittelinteraktionen. In der klinischen Praxis wird Ciclosporin insbesondere bei schwerer csU und/oder einem Typ-IIb-Phänotyp erwogen [1].
Persistieren die Symptome trotz hochdosierter Antihistaminikatherapie, sollte eskaliert werden.
Neue Therapieoptionen
Seit November 2025 neu zugelassen zur Therapie der csU ist Dupilumab, ein vollständig humaner monoklonaler Antikörper, der die gemeinsame Rezeptoruntereinheit von IL-4 und IL-13 (IL-4Rα) blockiert und damit die Signalgebung beider Schlüsselzytokine der Typ-2-Inflammation hemmt [10]. In randomisierten klinischen Studien bei Patienten und Patientinnen mit csU konnte Dupilumab eine signifikante Reduktion der Krankheitsaktivität, insbesondere von Juckreiz und Quaddelbildung, zeigen (CUPID A und C) [12].
Remibrutinib ist ein hochselektiver oraler Inhibitor der Bruton-Tyrosinkinase (BTK), einem zentralen Signalmolekül in FcεRI-vermittelten Aktivierungswegen von Mastzellen und Basophilen. In den großen Phase-III-Studienprogrammen REMIX-1 und REMIX-2 führte Remibrutinib zu signifikanten Verbesserungen eines kombinierten Pruritus- und Quaddel-Endpunkts bereits nach 12 Wochen Therapie [13]. Darüber hinaus liegen Daten zur Aufrechterhaltung der Wirksamkeit über 52 Wochen vor [14]. Remibrutinib ist in den USA seit September 2025 zur Behandlung der csU zugelassen, die EU-Zulassung ist beantragt.
Die deutsche S3-Leitlinie zur Klassifikation, Diagnostik und Therapie der Urtikaria [15] befindet sich in Überarbeitung. Es ist davon auszugehen, dass die neue Version die dann aktuell zugelassenen Medikamente als Option für die Zweitlinie empfehlen wird (Abb. 3).


Die csU ist eine heterogene, mastzellgetriebene Erkrankung, bei der eine standardisierte Diagnostik, objektive Aktivitäts-/Kontrollmessung und leitlinienbasierte Eskalation die Versorgungsqualität unmittelbar verbessern. Während Omalizumab weiterhin der zentrale Biologika-Standard bleibt, markieren Dupilumab und Remibrutinib eine relevante Erweiterung des therapeutischen Spektrums.
