

Dienogest/Estradiolvalerat (DNG / E2V) vereint als kombiniertes orales Kontrazeptivum (KOK) positive Effekte bei Androgenisierungserscheinungen mit einer vergleichsweise geringen Induktion von Gerinnungsfaktoren verglichen mit KOK, welche EE enthalten. Dielera® ist eine preisattraktive Alternative zum Originalpräparat.*
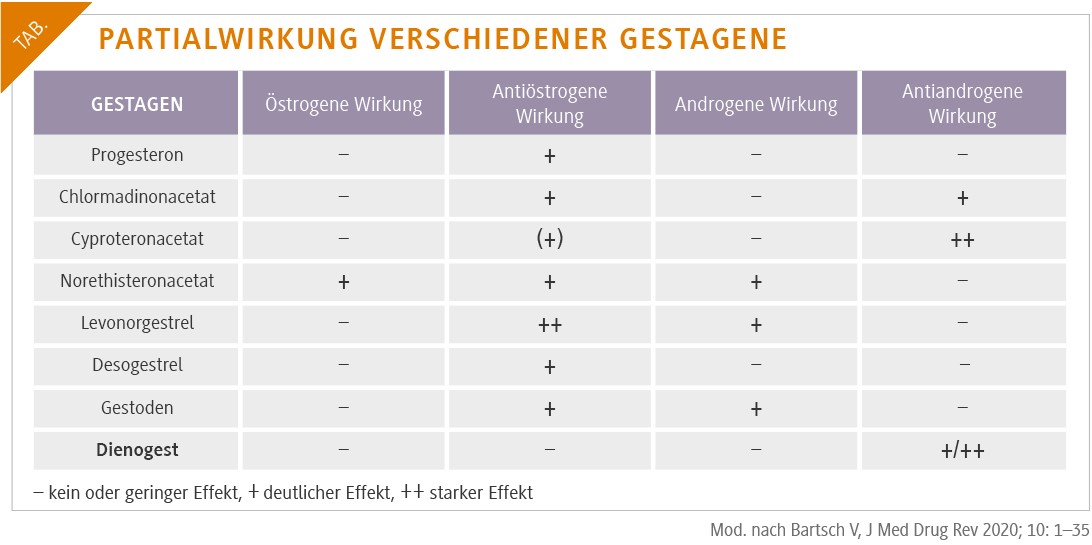
Estradiolvalerat (E2V) ist der Valeratester von 17β-Estradiol (E2) und wird nach oraler Applikation rasch zu E2 hydrolysiert [1,2]. Dienogest (DNG) ist ein 19-Nortestosteron-Derivat mit ausgeprägter endometrialer Potenz und hoher oraler Bioverfügbarkeit (> 90 %) und anti-androgenen Eigenschaften (Tab.) [3-5].
Das Präparat wird in einem 26/2-Regime appliziert (26 Tage wirkstoffhaltige Tabletten, 2 Tage Placebo) mit Estrogen-Step-down- und Gestagen-Step-up-Strategie: 2 Tage E2V 3 mg, 5 Tage E2V 2 mg/DNG 2 mg, 17 Tage E2V 2 mg/DNG 3 mg, 2 Tage E2V 1 mg, gefolgt von 2 Tagen Placebo (Abb. 1) [6,7]. Dieses Dosiskonzept gewährleistet eine initiale Estrogendominanz zur Stabilisierung des Endometriums und eine suffiziente Gestagendominanz in der Lutealphase zur Ovulationshemmung [8].

Pharmakokinetik
Unter E2V/DNG werden relativ konstante Serumspiegel von E2 über den 28-Tage-Zyklus erreicht; minimale mittlere E2-Konzentrationen während der Einnahme lagen im Bereich von 33,6 – 64,7 pg/ml, vergleichbar mit der mittleren Follikelphase des Spontanzyklus [2]. Die terminale Halbwertszeit von DNG beträgt etwa 12 h, Tmax liegt bei ca. 1,5 h [2]. SHBG steigt moderat (≈ 40 %), verbleibt jedoch im Normbereich; Cortisol-bindendes Globulin bleibt weitgehend unverändert [2].
Im Vergleich zu Ethinylestradiol (EE)-haltigen KOK zeigt E2 eine geringere hepatische Induktion von Proteinsynthese, einschließlich SHBG und Angiotensinogen [9]. Auch Effekte auf Gerinnungsmarker erscheinen weniger ausgeprägt als unter EE [10].
Kontrazeptive Wirksamkeit
In einer europäischen Phase-III-Studie mit 1 377 Frauen (20 Zyklen) betrug der adjustierte Pearl-Index 0,34 (95%-KI Obergrenze 0,73) [11]. Gepoolte Analysen aus drei Phase-III-Studien ergaben einen typischen Pearl-Index von 0,79 (95%-KI Obergrenze 1,23) und einen perfekten Pearl-Index von 0,42 (95%-KI Obergrenze 0,77) bei Frauen zwischen 18 und 50 Jahren [12]. Eine randomisierte Vergleichsstudie versus EE 20 µg/Levonorgestrel 100 µg (n = 798) zeigte eine vergleichbare kontrazeptive Sicherheit; eine Schwangerschaft trat in der Vergleichsgruppe auf [8].
Zyklus- und Blutungskontrolle
Die geplante Entzugsblutung trat unter E2V/DNG in 77,7– 83,2 % der Zyklen auf, unter EE/LNG in 89,5 – 93,8 % [8]. Dauer und Intensität der Entzugsblutung waren unter E2V/DNG signifikant reduziert (mittlere Dauer 4,1– 4,7 vs. 5,0 – 5,2 Tage; p < 0,05)*. Die Rate intrazyklischer Blutungen war vergleichbar (10,5 –18,6 % vs. 9,9 –17,1 %). Therapieabbrüche aufgrund von Blutungsstörungen waren mit 2,5 % niedrig [11].
Metabolische Effekte
In randomisierten Studien zeigte E2V/DNG im Vergleich zu EE/LNG vergleichbare oder günstigere Effekte auf Lipidparameter, Insulinsensitivität und Kohlenhydratmetabolismus [13]. Veränderungen von Prothrombinfragment 1 + 2 und D-Dimer waren gering [14]. Auch die thrombingenerierende Aktivität und APC-Sensitivität zeigten keine über das bekannte Klasseneffektprofil hinausgehenden Veränderungen [14,15]. Potenzielle Zusatznutzen umfassen Verbesserungen hormonentzugsassoziierter Symptome, primäre Dysmenorrhö und orale Kontrazeptiva-assoziierte sexuelle Dysfunktion [16-18].
Sicherheitsprofil
Das Sicherheitsprofil entspricht im Wesentlichen dem eines niedrig dosierten KOK. Aufgrund der Verwendung von E2 statt EE besteht theoretisch eine geringere hepatische Induktion und möglicherweise ein günstigeres metabolisches Profil [19,20].
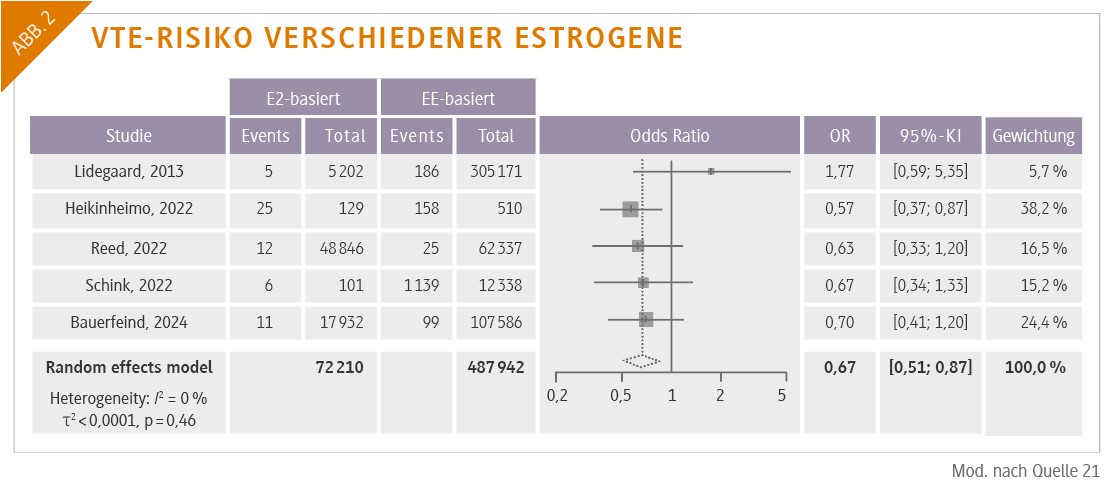
Eine Metaanalyse von 2024 identifizierte klinische Studien, in denen das VTE-Risiko von KOKs mit synthetischen und natürlichen Östrogenen verglichen wurde. Die Studien wurden durch ein strenges Screening ausgewählt, und die Datenextraktion erfolgte nach standardisierten Protokollen, wobei die statistischen Analysen unter Verwendung eines Random-Effects-Modells durchgeführt wurden [21]. Die Suche ergab fünf relevante Studien mit über 560 000 Frauen/Zeitpunkt, die eine signifikante Verringerung des VTE-Risikos um 33 % bei Anwenderinnen von KOKs auf Basis natürlicher Östrogene im Vergleich zu solchen auf Basis synthetischer Östrogene zeigten (OR 0,67; 95%-KI 0,51– 0,87). Stratifizierungsanalysen unter Verwendung adjustierter Hazard Ratios (HR) der wichtigsten Beobachtungsstudien zeigten ein um 49 % reduziertes VTE-Risiko von E2-basierten Pillen im Vergleich zu EE in Verbindung mit Levonorgestrel (Abb. 2). Die Verfügbarkeit der bewährten Kombination als Generikum sorgt für eine preiswerte Alternative zum Originalpräparat*.


DNG/E2V repräsentiert ein kombiniertes orales Kontrazeptivum mit natürlichem Estrogen und dynamischem Dosierungsschema. Es bietet eine hohe kontrazeptive Wirksamkeit bei akzeptabler Zykluskontrolle und signifikant reduzierter Blutungsintensität im Vergleich zu klassischen EE-haltigen Präparaten*. Das metabolische Profil erscheint im Vergleich zu EE-haltigen KOK günstig, was aktuelle Metaanalysen belegen.


Pflichttext
Dielera® Filmtabletten (Rp) Wirkstoffe: Estradiolvalerat/Dienogest
Zus.: dunkelgelbe Tabl.: 3 mg Estradiolvalerat; pinke Tabl.: 2 mg Estradiolvalerat und 2 mg Dienogest; hellgelbe Tabl.: 2 mg Estradiolvalerat und 3 mg Dienogest; braune Tabl.: 1 mg Estradiolvalerat; weiße Tabl: ohne Wirkstoffe. Sonst. Bestandt.: Lactose-Monohydrat, Maisstärke, Vorverkleisterte Stärke (Mais), Povidon K25 (E1201), Hochdisperses Siliciumdioxid, Magnesiumstearat (Ph. Eur.) [pflanzlich] (E572), Hypromellose (E464), Macrogol 6000, Titandioxid (E171), Talkum (E553b), Eisen(III)-hydroxid-oxid x H2O (E172), Eisen(III)-oxid (E172), Mikrokristalline Cellulose [Ph. Eur], Poly(vinylalkohol), partiell hydrolysiert, Macrogol 3350. Anw.: Orale Kontrazeption. Bei der Entscheidung, Dielera® zu verschreiben, sollten die aktuellen, individuellen Risikofaktoren der einzelnen Frauen, insbesondere im Hinblick auf venöse Thromboembolien (VTE), berücksichtigt werden. Auch sollte das Risiko für eine VTE bei Anwendung von Dielera® mit dem anderer kombinierter hormonaler Kontrazeptiva (KHK) verglichen werden. Gegenanz.: Vorliegen einer oder Risiko für eine venöse Thromboembolie (VTE); Venöse Thromboembolie – bestehende VTE (auch unter Therapie mit Antikoagulanzien) oder VTE in der Vorgeschichte (z. B. tiefe Venenthrombose [TVT] oder Lungenembolie [LE]); Bekannte erbliche oder erworbene Prädisposition für eine venöse Thromboembolie, wie z. B. APC-Resistenz (einschließlich Faktor-V-Leiden), Antithrombin-III-Mangel, Protein-C-Mangel oder Protein-S-Mangel; Größere Operationen mit längerer Immobilisierung; Hohes Risiko für eine venöse thromboembolie aufgrund mehrerer Risikofaktoren; Vorliegen einer oder Risiko für eine arterielle Thromboembolie (ATE); Arterielle Thromboembolie – bestehende ATE, ATE in der Vorgeschichte (z. B. Myokardinfarkt) oder Erkrankung im Prodromalstadium (z. B. Angina pectoris); Zerebrovaskuläre Erkrankung – bestehender Schlaganfall, Schlaganfall oder prodromale Erkrankung (z. B. transitorische ischämische Attacke [TIA]) in der Vorgeschichte; Bekannte erbliche oder erworbene Prädisposition für eine arterielle Thromboembolie, wie z. B. Hyperhomocysteinämie und Antiphospholipid-Antikörper (Anticardiolipin-Antikörper, Lupusantikoagulans); Migräne mit fokalen neurologischen Symptomen in der Vorgeschichte; Hohes Risiko für eine arterielle Thromboembolie aufgrund mehrerer Risikofaktoren oder eines schwerwiegenden Risikofaktors wie: Diabetes mellitus mit Gefäßschädigung, Schwere Hypertonie, Schwere Dyslipoproteinämie; Bestehende oder vorausgegangene schwere Lebererkrankung, solange sich die Leberfunktionswerte nicht normalisiert haben, Bestehende oder vorausgegangene Lebertumoren (benigne oder maligne), Bekannte oder vermutete sexualhormonabhängige maligne Tumoren (z. B. der Genitalorgane oder der Brust); Diagnostisch nicht abgeklärte vaginale Blutungen; Überempfindlichkeit gegen die Wirkstoffe oder einen der sonstigen Bestandteile. Nebenw: Häufig: Kopfschmerzen, abdominale Schmerzen, Übelkeit, Akne, Amenorrhoe, Brustbeschwerden, Dysmenorrhoe, Zwischenblutungen (Metrorrhagie), Gewichtszunahme. Gelegentlich: Pilzinfektion, mykotische vulvovaginale Infektion, vaginale Infektion, verstärkter Appetit, Depression/depressive Verstimmung, emotionale Störung, Schlaflosigkeit, verminderte Libido, psychische Störung, Stimmungswechsel, Benommenheit, Migräne, Hitzewallung, Hypertonie, Diarrhoe, Erbrechen, Anstieg der Leberenzyme, Alopezie, Hyperhidrosis, Pruritus, Hautausschlag, Muskelkrämpfe, Brustvergrößerung, Raumforderung in der Brust, Zervixdysplasie, dysfunktionelle uterine Blutungen, Dyspareunie, fibrozystische Brustveränderungen, Menorrhagie, Menstruationsstörungen, Ovarialzysten, Beckenschmerzen, prämenstruelles Syndrom, Uterusleiomyom, Uteruskrämpfe, uterine/vaginale Blutungen einschließl. Schmierblutung, vaginaler Ausfluss, vulvovaginale Trockenheit, Müdigkeit, Reizbarkeit, Ödeme, Gewichtsabnahme, Blutdruckveränderungen. Selten: Candidiasis, oraler Herpes, PID (Unterleibsentzündung), vermutetes okuläres Histoplasmose-Syndrom, Tinea versicolor, Harnwegsinfektion, bakterielle Vaginitis, Flüssigkeitsretention, Hypertriglyzeridämie, Aggression, Angst, Dysphorie, verstärkte Libido, Nervosität, Alptraum, Unruhe, Schlafstörung, Stress, Aufmerksamkeitsstörung, Parästhesie, Vertigo, Kontaktlinsenunverträglichkeit, trockene Augen, Augenschwellung, Myokardinfarkt, Palpitationen, blutende Varizen, venöse Thromboembolie (VTE), arterielle Thromboembolie (ATE), Hypotonie, Thrombophlebitis, Venenschmerzen, Obstipation, Mundtrockenheit, Dyspepsie, gastroösophageale Refluxerkrankung, fokal noduläre Hyperplasie der Leber, chronische Cholezystitis, allergische Hautreaktion, Chloasma, Dermatitis, Hirsutismus, Hypertrichose, Neurodermitis, Pigmentationsstörung, Seborrhoe, Hauterkrankung, Rückenschmerzen, Kieferschmerzen, Schweregefühl, Schmerzen im Bereich des Harntrakts, ungewöhnliche Abbruchblutungen, benigne Brustneoplasien, Mammakarzinom in situ, Brustzysten, Brustsekretion, zervikale Polypen, zervikales Erythem, koitale Blutungen, Galaktorrhoe, genitaler Ausfluss, Hypomenorrhoe, verspätete Menstruation, rupturierte Ovarialzyste, Vaginalgeruch, vulvovaginales Brennen, vulvovaginale Beschwerden, Lymphadenopathie Asthma, Dyspnoe, Epistaxis, Schmerzen im Brustkorb, Unwohlsein, Pyrexie, pathologischer Zervixabstrich. Enthält Lactose. Packungsbeilage beachten. (verschreibungspflichtig). (Stand Dezember 2024). Aristo Pharma GmbH, Wallenroder Straße 8-10, 13435 Berlin.
* Dielera® ist zugelassen zur Kontrazeption, nicht jedoch zur Behandlung der Hypermenorrhö.
Impressum
Bericht I Redaktion I Konzept: Dr. rer. nat. Reinhard Merz
MiM Verlagsgesellschaft mbH (Neu-Isenburg)
Mit freundlicher Unterstützung der Aristo Pharma GmbH (Berlin)
Bildnachweis: privat