

Für viele Patientinnen unter Chemotherapie gehört der Haarausfall zu den schlimmsten Nebenwirkungen. Hilotherapie kann helfen, ist in Deutschland aber keine Kassenleistung. Dieser Beitrag beschreibt ein Modell zum Betrieb und zur Abrechnung.
Die Chemotherapie-induzierte Alopezie (Chemotherapy-induced alopecia, CIA) ist eine häufige Nebenwirkung der Chemotherapie, insbesondere bei Patientinnen mit Mammakarzinom, die mit Taxanen und/oder Anthrazyklinen behandelt werden. Die kontrollierte Kühlung zur Reduktion des Chemotherapie-induzierten Haarausfalles ist seit Jahren bekannt. Das Konzept wurde in den vergangenen Jahren weiterentwickelt und verbessert und ist ein wichtiger Ansatz zum Erhalt der Lebensqualität onkologischer Patientinnen in der Gynäkologie. Daten aus randomisierten Studien belegen, dass die Hilotherapie effektiv ist [1-3].
Physiologisch beruht das Verfahren auf einer lokal induzierten Halbtiefen-Hypothermie der Kopfhaut während und nach Applikation der Zytostatika. Durch die Vasokonstriktion wird die regionale Perfusion reduziert, wodurch die zytotoxische Substanzkonzentration im Bereich der Haarfollikel sinkt. Gleichzeitig wird der Zellmetabolismus der Matrixzellen verlangsamt, sodass die Anfälligkeit gegenüber proliferationsabhängigen Chemotherapeutika abnimmt. Klinische Erfahrungen zeigen, dass sich hierdurch das Risiko für eine ausgeprägte CIA signifikant reduzieren lässt, was für viele Patientinnen ein entscheidendes Kriterium bei der Wahl des Behandlungszentrums darstellt.
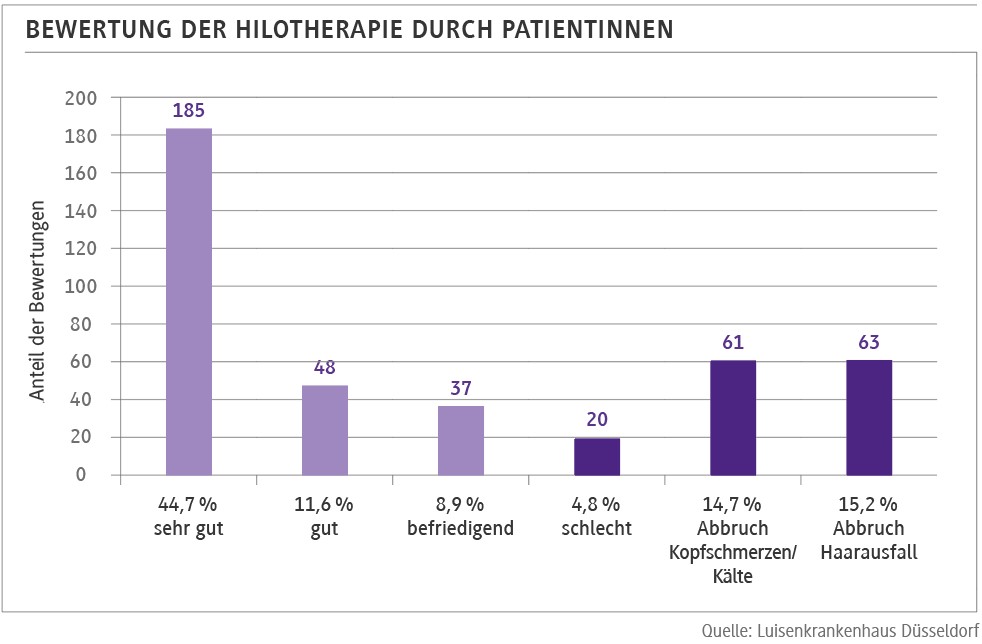
In vielen nationalen sowie internationalen onkologischen Kliniken und Praxen hat sich das kontrollierte Kühlverfahren bereits als Supportivtherapie etabliert. Die Ergebnisse einer Erhebung zur Hilotherapie bei 414 Patientinnen des Luisenhospitals Düsseldorf sind in Abb. 1 dargestellt.
Die CIA wird oft als temporäre Nebenwirkung betrachtet [4]. Wenig Beachtung findet die Tatsache, dass nach Abschluss der Chemotherapie das erneute Wachstum der Haare bei einem Teil der Patientinnen Monate oder Jahre auf sich warten lässt. Daraus kann eine lang andauernde vollständige oder inkomplette Alopezie resultieren. Diese Variante des langfristigen Haarausfalls wird als persistierende CIA bezeichnet (persistent Chemotherapy-induced alopecia, PCIA) [5]. In einer prospektiven Studie hatten 42,3 % der Patientinnen mit Mammakarzinom 3 Jahre nach der Chemotherapie ein unvollständiges Wiederwachstum [6].
Herausforderungen für die Praxis
In der praktischen Umsetzung stellt die Integration der Hilotherapie in den Praxis- oder Klinikalltag jedoch eine logistische Herausforderung dar. Der Betreuungsaufwand ist erhöht, da viele Patientinnen beim Anlegen und Justieren der Kühlhauben Unterstützung benötigen und während der Therapie engmaschiger überwacht werden müssen. Hinzu kommen räumliche Anforderungen, da die Behandlungszimmer häufig nicht für die zusätzliche Gerätetechnik ausgelegt sind. Der zeitliche Mehraufwand durch die notwendigen Vor- und Nachkühlzeiten ist ebenfalls zu berücksichtigen. Moderne tragbare Module ermöglichen jedoch eine Nachkühlung an einem anderen Ort, was die Raumnutzung flexibler gestaltet und den Durchsatz im Chemotherapiebereich verbessert.
Abrechnung
In Deutschland ist die Hilotherapie zur CIA-Prophylaxe derzeit noch keine allgemeine Regelleistung der gesetzlichen Krankenversicherung. Private Krankenversicherungen übernehmen die Kosten jedoch in der Regel im Rahmen einer analogen Abrechnung nach GOÄ-Ziffer A 5853, die ursprünglich für die Oberflächen- bzw. Halbtiefen-Hyperthermie vorgesehen ist. Die analoge Anwendung erfolgt gemäß § 6 Abs. 2 GOÄ für die Halbtiefen-Hypothermie der Kopfhaut unter Chemotherapie und wird aktuell mit 116,57 Euro pro Sitzung bewertet. Trotz fehlender Regelversorgung steigt die Nachfrage kontinuierlich, und es ist zu beobachten, dass Patientinnen gezielt Kliniken und onkologische Schwerpunktpraxen aufsuchen, die eine Kopfhautkühlung anbieten.
Die Finanzierung der Geräte ist ein zentraler Aspekt bei der Implementierung. Viele Patientinnen mieten die Systeme inzwischen direkt beim Hersteller und tragen die Kosten in Höhe von etwa 995 Euro eigenständig, sofern keine Kostenübernahme durch ihre Versicherung erfolgt. Alternativ entscheiden sich immer mehr Praxen und Kliniken für Leasing- oder Mietmodelle mit einer Laufzeit von beispielsweise 3 Jahren, was mit monatlichen Kosten von rund ca. 250 Euro zuzüglich Mehrwertsteuer verbunden ist. Unter wirtschaftlichen Gesichtspunkten kann sich die Anschaffung bereits bei einer privatversicherten Patientin pro Monat amortisieren, etwa bei wöchentlicher Paclitaxel-Therapie oder bei EC-Schemata im zweiwöchentlichen Intervall.
Aus ökonomischer Sicht bietet die Hilotherapie für Praxen und Kliniken die Möglichkeit, eine zusätzliche Eigenleistung zu etablieren, die mit 50 bis 100 Euro pro Sitzung berechnet wird und damit sowohl für die Patientinnen eine kostengünstigere Alternative zur Einzelmiete als auch für die Einrichtung eine zusätzliche Einnahmequelle darstellt.
Die NATUM besitzt ein Gerät zur Hilotherapie. Dies kann für 3 Monate von der NATUM kostenfrei zur Verfügung gestellt werden. So können interessierte Kliniken und Praxen ohne finanzielle Investition die Lebensqualität der Erkrankten verbessern, eigene Erfahrungen gewinnen und zusätzliche Einnahmen generieren. Beispiele zu Abrechnungsmöglichkeiten bei weiteren komplementärmedizinischen Leistungen sind im Abrechnungskurs der NATUM zusammengestellt: https://www.natum-veranstaltungen.de/e-learning
Der Autor

Prof. Dr. med. Harald Meden
Facharzt für Gynäkologie und Geburtshilfe
Swiss Institute for New Concepts and Treatments (SINCT)
Die Autorin

Dr. rer. nat. Trudi Schaper
Zentrum für Gynäkologische Onkologie am Luisenkrankenhaus
40235 Düsseldorf
trudi.schaper@luisenkrankenhaus.de
Bildnachweis: privat