

Licht ist ein zentraler Umweltfaktor bei dermatologischen Indikationen wie Sonnenbrand, Photodermatosen, Virusreaktivierung und Karzinogenese. Dieser Beitrag gibt einen aktuellen Überblick über Pathomechanismen, Klinik und Prävention lichtinduzierter Hautschädigung.
Für die Haut sind aus dem Spektrum elektromagnetischer Strahlung ultraviolette (UV) Strahlung, sichtbares Licht (VIS) und Infrarotstrahlung (IR) relevant. Aufgrund der Filterwirkung der Atmosphäre erreichen vor allem UV-A (320 – 400 nm) und UV-B (280 –320 nm)-Strahlen die Erdoberfläche [1].
UV-B ist energiereicher und spielt eine Schlüsselrolle bei akuten Effekten wie Sonnenbrand (Dermatitis solaris) sowie bei direkter DNA-Schädigung. UV-B trägt maßgeblich zur extrinsischen Hautalterung (Photoaging) und zur Karzinogenese bei. UV-A dringt tiefer in die Haut ein und wirkt überwiegend indirekt über oxidative Mechanismen [2].
Auch sichtbares Licht kann potenziell zur vorzeitigen Hautalterung beitragen [3]. Reviews beschreiben zudem photorezeptorvermittelte und ROS (reaktive Sauerstoff-Spezies)-abhängige Mechanismen sichtlichtinduzierter Photoaging-Prozesse. Besonders relevant sind Pigmentantworten und Entzündungsmediatoren [4,5]. Für IR-A werden mitochondriale Stressantworten, thermische Signaltransduktion und nachgeschaltete Matrixveränderungen (u. a. MMP-Achsen) als Mechanismen diskutiert [5,6].
Pathophysiologie
Die Gewebepenetration ist wellenlängenabhängig: UV-B wird weitgehend in der Epidermis absorbiert, UV-A dringt bis in die obere/mittlere Dermis vor. VIS und IR-A können tiefer eindringen; IR-A erreicht dermale und subdermale Kompartimente und wirkt insbesondere über thermische und mitochondriale Mechanismen [3-5] (Abb. 1). Klinisch und pathogenetisch zentral sind 4 Zielsysteme:
Die Haut verfügt über eine adaptive Photoprotektion durch Zunahme der Epidermisdicke (Akanthose/Hyperkeratose; „Lichtschwiele“), Melanogenese, antioxidative Systeme sowie DNA-Reparatur (v. a. Nukleotid-Exzisionsreparatur). Diese Mechanismen erklären die klinische Beobachtung, dass chronisch belichtete Areale (Gesicht, Handrücken) gegenüber bestimmten Photodermatosen eine relative „Gewöhnung“ aufweisen [2,7].
UV-B induziert direkt photochemische DNA-Schäden (v. a. Cyclobutan-Pyrimidin-Dimere) und triggert p53-abhängige Signalwege; „sunburn cells“ reflektieren apoptotische Keratinozyten. UV-A erzeugt überwiegend indirekte Schäden über ROS (z. B. oxidative DNA-Schäden, Lipidperoxidation, Proteinoxidation), fördert entzündliche und matrixdegradierende Signalwege und trägt wesentlich zu Photoaging bei [2,6,8].

Dermatitis solaris
Diese akute toxische Hautschädigung ist überwiegend UV-B-getriggert, mit schmerzhafter Rötung und – bei schwerem Verlauf – Blasenbildung (Abb. 2). Typischerweise tritt das Maximum des Erythems zeitverzögert auf (klassisch 12–24 Stunden), mit Abklingen nach einigen Tagen. Histologisch finden sich epidermale Apoptosen („sunburn cells“) und dermale Entzündungsinfiltrate [2].
Therapeutisch stehen symptomatische Maßnahmen wie Kühlung, topische entzündungshemmende Therapie und Analgesie im Vordergrund. Bei schweren Verläufen können systemische Antiphlogistika indiziert sein. Wichtig ist die Aufklärung über konsequenten Schutz. Dazu gehören physikalischer Textilschutz, breitbandige Sonnenschutzpräparate (UV-B/UV-A) und entsprechende Verhaltensmaßnahmen. Für die Wirksamkeit von Sonnenschutz ist die ausreichende Auftragsmenge klinisch entscheidend. Häufig wird unterdosiert, was den effektiven Schutz deutlich reduziert [2].
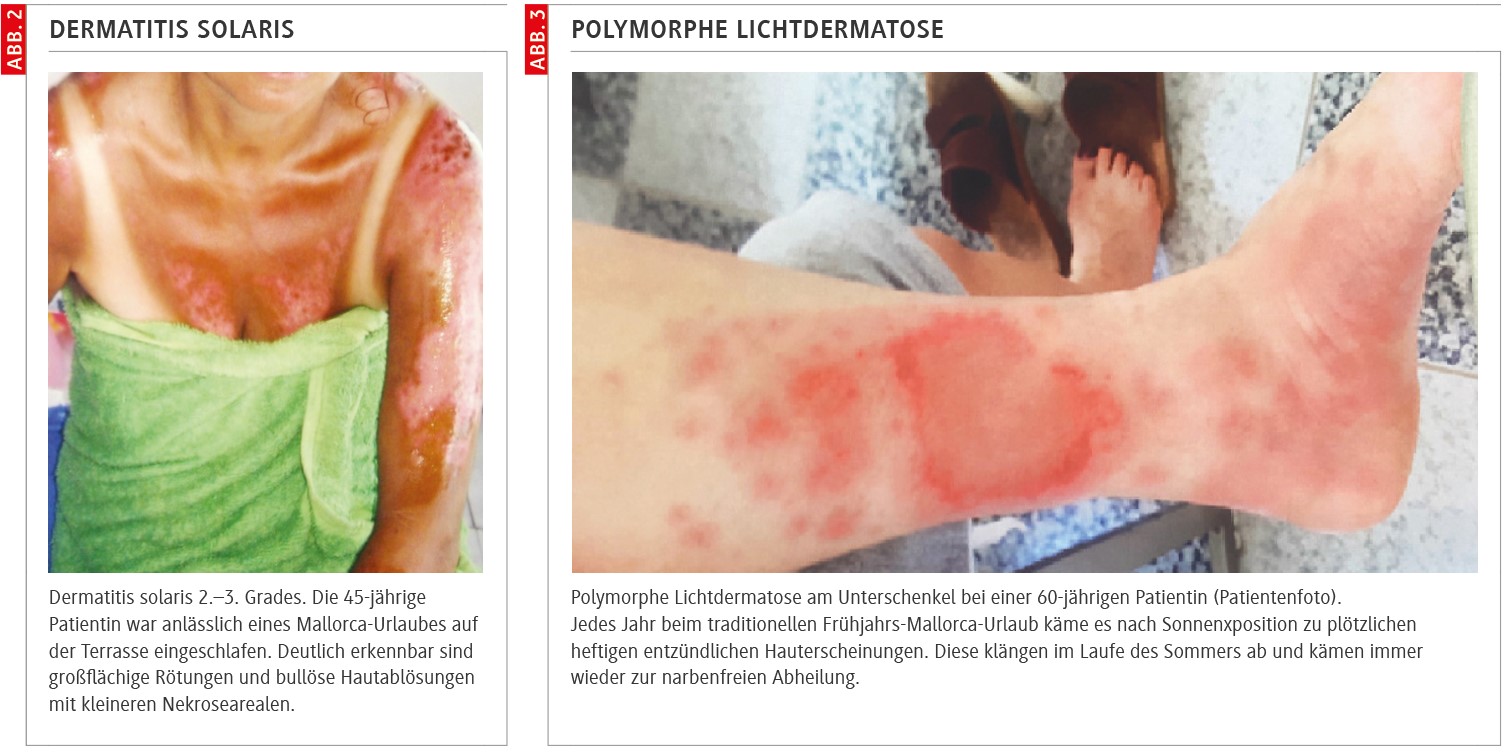
Polymorphe Lichtdermatose (PLD)
Die PLD ist die häufigste idiopathische Photodermatose. Klinisch charakteristisch sind juckende, polymorphe Effloreszenzen (Papeln, Vesikel, Plaques) Stunden bis Tage nach einer ersten intensiven Sonnenexposition, etwa im Frühjahr oder im Urlaub. Die Effloreszenzen treten bevorzugt an Hals, Dekolleté, Armen und Oberschenkeln auf, oft mit relativer Gesichtsaussparung (Abb. 3). Viele Patientinnen und Patienten zeigen im Verlauf des Sommers eine Gewöhnung („hardening“), sodass die Läsionen trotz fortgesetzter Exposition abklingen [7]. Die Prävalenz der PLD liegt im Bereich von 10 bis 20 % [9].
Obwohl die Pathogenese der PLD nicht abschließend geklärt ist, wird ein multifaktorielles Geschehen vermutet. So stellt das aufgrund der reduzierten Clearance der apoptotischen Zellen nicht abgebaute Zellmaterial nach UV-Exposition eine mögliche Autoantigenquelle dar. Gleichzeitig findet sich in der Haut der PLD-Patienten und -Patientinnen nach UV-Exposition eine signifikant höhere Anzahl an Langerhans-Zellen als in der Haut gesunder Personen [7]. Proinflammatorische Zytokine der IL-1-Familie (IL-36α und IL-36γ) werden vermehrt exprimiert [10].
Die Läsionen treten rasch nach UV-Exposition auf und heilen nach dem Meiden von Sonnenlicht schnell wieder ab. Die Diagnose PLD kann histologisch und mittels Lichtprovokation bestätigt werden. Dabei werden auf der lichtexponierten Haut wiederholt Bestrahlungen durchgeführt, um die Hautveränderungen zu reproduzieren [7].
Zur Therapie der akuten Läsionen kommen topische Kortikosteroide zum Einsatz. Um dem Auftreten der Hautveränderungen vorzubeugen, werden textiler Lichtschutz bzw. die Anwendung von Lichtschutzcremes mit besonders hohem UV-B- und UV-A-Schutz empfohlen. In ausgeprägten Fällen kann den Betroffenen eine Lichtgewöhnungstherapie im Sinne eines UV- „hardenings“ vor Beginn der intensiven Sonneneinstrahlung angeboten werden [7]. Für eine therapieresistente PLD können in Ausnahmefällen auch immunmodulierende Wirkstoffe erwogen werden.
Lichturtikaria (Urticaria solaris)
Lichturtikaria ist selten, kann aber schwere Verläufe bis zur Anaphylaxie verursachen. Typisch sind erythematöse Quaddeln Minuten nach Belichtung mit rascher Rückbildung binnen 30 – 60 Minuten [2]. Das Aktionsspektrum variiert. Häufig ist UV-A beteiligt, möglich sind aber auch UV-B und sichtbares Licht.
Pathophysiologisch wird überwiegend eine IgE-vermittelte Soforttypreaktion gegen ein photoaktiviertes endogenes Antigen angenommen; Mastzellaktivierung und Histaminfreisetzung stehen im Vordergrund [7]. Neuere Arbeiten weisen zusätzlich auf signalwegbezogene Veränderungen hin (z. B. frühe STAT3-Aktivierung, Rekrutierung angeborener Effektorzellen), was die Krankheit als mehrschichtiges Entzündungssyndrom plausibilisiert [11].
Diagnostisch wird die Photoprovokation mit UV-A/UV-B und sichtbarem Licht eingesetzt, zur Bestimmung der minimalen urtikariellen Dosis (MUD) via Lichttreppe [7]. Zur Therapie existiert ein Stufenschema (Abb. 4). Es umfasst konsequenten Lichtschutz, hochdosierte (bis zu 4-fache Dosis) nicht-sedierende H1-Antihistaminika (off-label) und – bei therapierefraktären Fällen – Omalizumab (off-label) sowie UV-A-(1)-Rush-Hardening in spezialisierten Zentren [7].

Sekundäre Photodermatosen
Die vorab beschriebenen primären Photodermatosen sind von sekundären Photodermatosen abzugrenzen, deren Photosensitivität durch Grunderkrankungen (Autoimmunität, Stoffwechselstörung, Enzymdefekte) bedingt ist [1].
Porphyrien sind heterogene Stoffwechselerkrankungen der Porphyrin-/Häm-Biosynthese. Die Akkumulation phototoxischer Porphyrine oder Vorstufen führt zu kutanen, neurokutanen oder nicht-kutanen Verlaufsformen; Lichtabsorption (v. a. UV-A / VIS) generiert ROS und verursacht Gewebsschädigung [1]. Klinisch wichtig sind:
Zur Diagnostik wird die biochemische Porphyrinanalytik in Urin, Stuhl und Blut herangezogen, ggf. mit molekulargenetischer Testung [1]. Zu den therapeutischen Maßnahmen zählt konsequenter Lichtschutz. Bei EPP ist Afamelanotid als moderne Therapieoption etabliert, bei PCT u. a. niedrig dosiertes Hydroxychloroquin als klassische Option [1].
Bei Lupus erythematodes (LE) führt UV-Exposition nicht zu der in gesunder Haut typischen Immunsuppression, sondern zu pathologischer Entzündungsaktivierung (Abb. 5). Diskutiert werden UV-induzierter oxidativer Stress, Keratinozytenapoptose und Autoantigenexposition. In der Folge werden die Rekrutierung von Neutrophilen und die Ausschüttung von proinflammatorischen Zytokinen verstärkt [1]. Klinisch entstehen Hautläsionen oft verzögert, Tage bis Wochen nach UV-Exposition. Therapeutisch ist neben konsequentem Lichtschutz die systemische Immunmodulation von zentraler Bedeutung.
Lichtinduzierte VZV-Reaktivierung
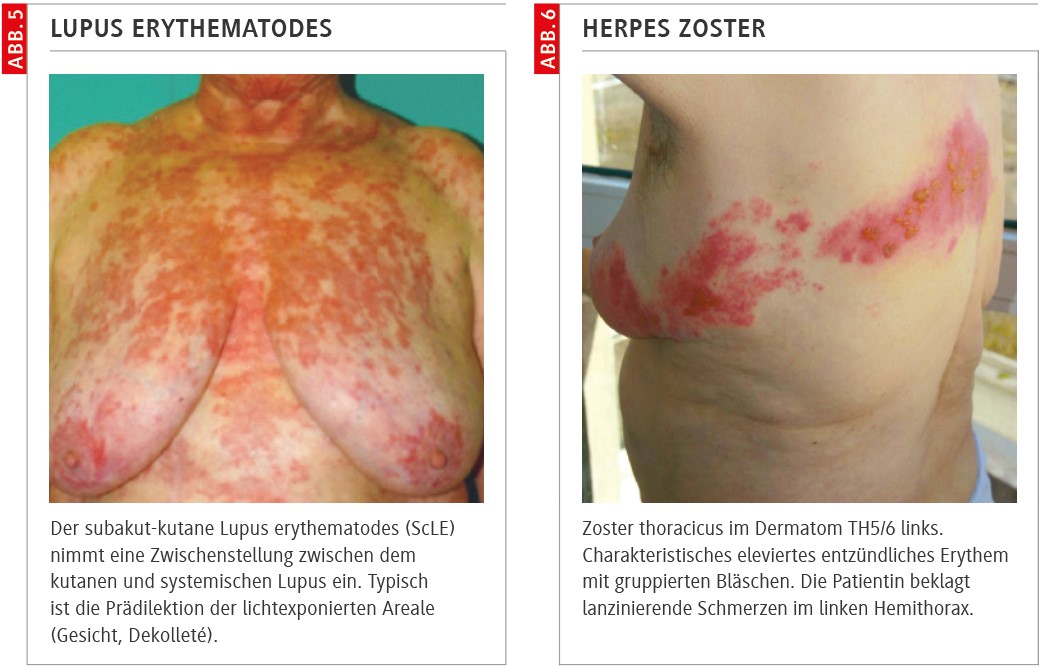
Das Varizella-zoster-Virus (VZV) persistiert nach Primärinfektion (Varizellen) lebenslang latent in den sensorischen Spinal- und Hirnnervenganglien. Die Reaktivierung führt klinisch zum Herpes zoster, charakterisiert durch segmental begrenzte, schmerzhafte vesikuläre Effloreszenzen entlang eines Dermatoms (Abb. 6). Neben bekannten Risikofaktoren wie höherem Lebensalter, Immunsuppression und systemischen Stressoren wird zunehmend auch UV-Strahlung als möglicher Trigger der VZV-Reaktivierung diskutiert [12,13].
Grund sind Beobachtungen über das Auftreten eines Herpes zosters bevorzugt in zuvor intensiv lichtexponierten Hautarealen sowie zeitlich assoziiert mit Sonnenexposition oder phototherapeutischen Maßnahmen. Besonders häufig betroffen sind Dermatomregionen im Gesichts- und Halsbereich. Diese Beobachtungen legen nahe, dass Licht – insbesondere UV-Strahlung – lokale oder systemische Mechanismen aktiviert, die die virale Latenz destabilisieren.
Pathophysiologisch werden mehrere Mechanismen diskutiert. UV-Strahlung führt in der Haut zu einer lokalen Immunsuppression, unter anderem durch funktionelle Beeinträchtigung epidermaler Langerhans-Zellen, Induktion regulatorischer T-Zellen und vermehrte Freisetzung immunsuppressiver Zytokine wie IL-10 [14]. Diese Effekte können jedoch die antivirale Immunüberwachung schwächen. Insbesondere die zelluläre Immunität, die für die Kontrolle der VZV-Latenz essenziell ist, scheint UV-induziert transient reduziert zu werden.
Therapeutisch gelten die etablierten antiviralen Regime (Aciclovir, Valaciclovir, Famciclovir), idealerweise innerhalb von 72 Stunden nach Auftreten der Effloreszenzen. Eine besondere Rolle kommt der Prävention zu: Neben konsequentem Lichtschutz ist die Zoster-Impfung (rekombinanter Totimpfstoff) eine effektive Maßnahme zur Reduktion von Inzidenz und Schweregrad des Herpes zosters, vor allem bei älteren und chronisch kranken Patientengruppen [15].
Die Rolle des Klimawandels
Der Klimawandel führt zu mehr warmen und wolkenlosen Tagen, was die Sonnenstunden und damit die UV-Exposition erhöht. Auch häufiger auftretende Niedrig-Ozon-Ereignisse können im Frühjahr zu unerwartet hoher UV-Belastung führen. Insgesamt wurde in den vergangenen 25 Jahren in Deutschland ein signifikanter Anstieg der UV-Strahlung um mehr als 10 % festgestellt [16].
Studien zeigen einen Anstieg atopischer Erkrankungen in Deutschland um ca. 30 % (Zahlen der BKK Nordwest, Stand 2021). Bei atopischer Dermatitis (AD) begünstigen Temperaturen über 25 °C Schübe, während extrem schwankende Luftfeuchtigkeit die Barrierefunktion der Haut kompromittiert und Symptome wie Trockenheit und Pruritus verschlimmert. Auch die klimabedingte Zunahme von Pollen und Luftschadstoffen kann AD-Schübe auslösen, indem sie entzündliche Prozesse der Hautbarriere fördert.
Risikofaktoren wie Hitze und Luftverschmutzung beschleunigen auch die Hautalterung. Eine indische Studie zeigt, dass ein höherer Hitze-Index Entzündungsprozesse auslöst sowie zu stärkerer Pigmentierung der Stirn, tieferen Falten und gröberen Hautstrukturen führt – unabhängig von Alter, Rauchen, UV-Strahlung oder Luftverschmutzung [17]. Last but not least verzeichnet das Statistische Bundesamt einen Anstieg sowohl bei Krankenhausbehandlungen als auch bei Sterbefällen im Zusammenhang mit Hautkrebs über einen Zeitraum von 20 Jahren.
FAZIT:
Durch den Klimawandel ändert sich auch die UV-Exposition – auch in unseren Breiten. Die daraus resultierenden primären und sekundären Photodermatosen müssen wir auf dem Schirm haben und Patienten sowie Patientinnen entsprechend beraten.
Der Autor

Dr. med. Viktor Alexander Czaika
Facharzt für Dermatologie,
Venerologie und Innere Medizin
12439 Berlin
Bildnachweis: About time (gettyimages), Dr. med. Viktor A. Czaika