

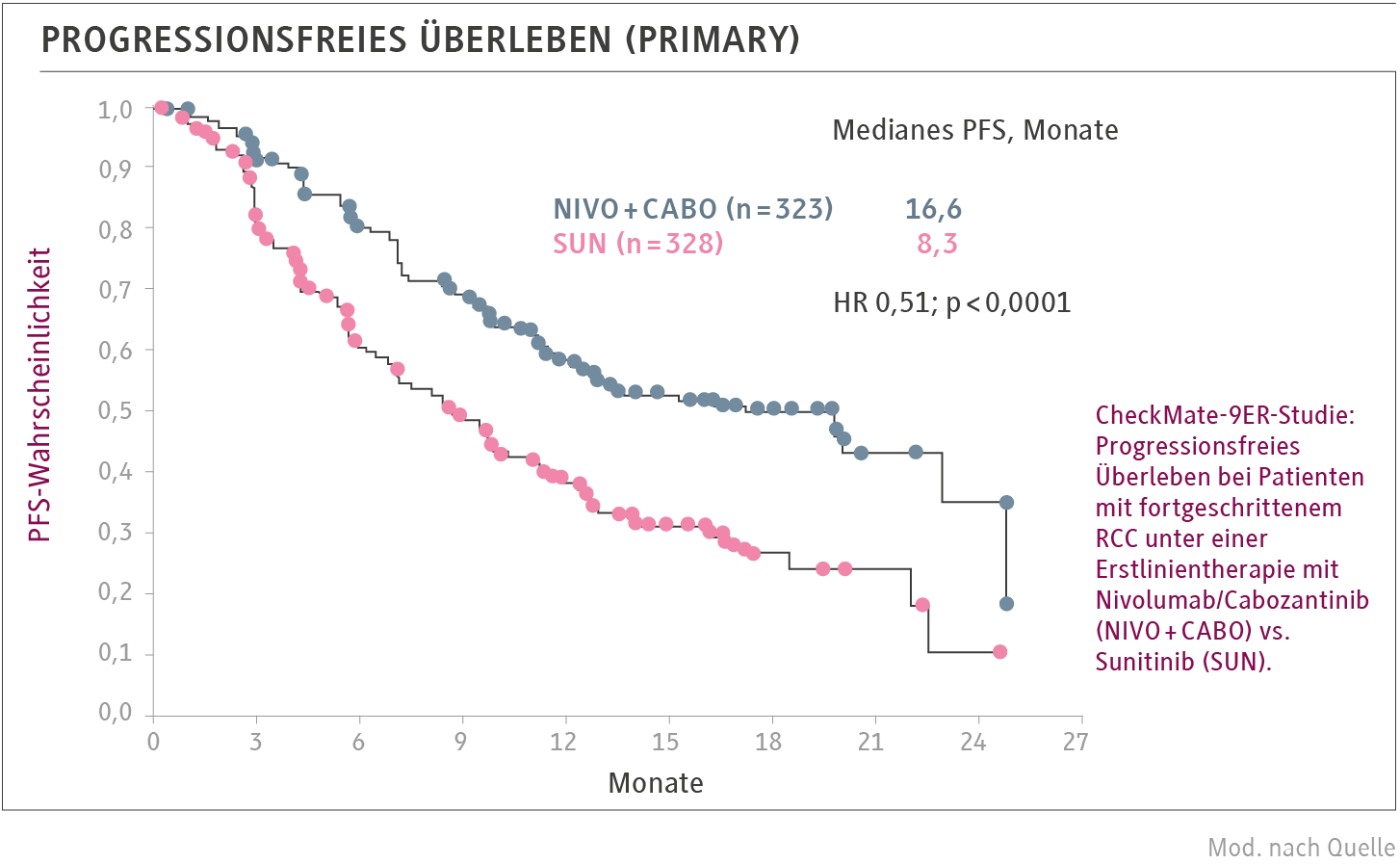
Eines der Highlights beim virtuellen ESMO-Kongress war die Vorstellung der Daten der Phase-III-Studie CheckMate 9ER zur Erstlinientherapie beim fortgeschrittenen Nierenzellkarzinom (RCC). Die Studienergebnisse zeigen eine deutliche Überlegenheit der Kombinationstherapie aus dem Checkpoint-Inhibitor Nivolumab und dem Tyrosinkinase-Inhibitor (TKI) Cabozantinib gegenüber dem früheren Therapiestandard Sunitinib hinsichtlich aller relevanten Wirksamkeitsendpunkte: Gesamtüberleben (OS), progressionsfreies Überleben (PFS) und Gesamtansprechrate (ORR).1 Es lag nahe, diese Kombination zu testen, da beide Substanzen zugelassene Therapien beim RCC sind und andere Kombinationen aus Checkpoint-Inhibitoren und TKI beim RCC bereits erfolgreich eingesetzt werden. Wie Studienleiter Dr. Toni Choueiri, Boston, MA, USA, im Presidential Symposium I beim ESMO berichtete, erhielten 651 Patienten mit nicht vorbehandeltem, fortgeschrittenem oder metastasiertem, klarzelligem RCC randomisiert entweder Nivolumab (240 mg i. v. alle zwei Wochen) plus Cabozantinib (40 mg oral täglich) oder Sunitinib in Standarddosierung. Primärer Endpunkt war das PFS. Im Kombinationsarm (n = 323) konnte eine 50%ige Risikoreduktion für Progress oder Tod vs. Sunitinib gezeigt werden, bei einem medianen PFS von 16,6 vs. 8,3 Monaten (HR 0,51; p < 0,0001). Auch die ORR war mit 55,7 % im Kombinationsarm fast doppelt so hoch wie unter Sunitinib mit 27,1 % – mit 8 ,0 % vs. 4,6 % kompletten und 47,7 % vs. 22,6 % partiellen Remissionen. Beim sekundären Endpunkt OS war die Kombination ebenfalls relevant überlegen mit einer HR von 0,60; das mediane OS war in beiden Armen noch nicht erreicht. Das Sicherheitsprofil der vergleichsweise intensiven Behandlung erwies sich als handhabbar. Die Inzidenz an behandlungsassoziierten Nebenwirkungen war in beiden Armen vergleichbar, die Rate an Behandlungsabbrüchen niedrig. Auch die gesundheitsbezogene Lebensqualität unter Nivolumab/Cabozantinib blieb erhalten, während sie sich im Sunitinib-Arm verschlechterte. Laut Choueiri sprechen die Daten der CheckMate-9ER-Studie dafür, dass die Kombination Nivolumab plus Cabozantinib in Zukunft ein neuer Erstlinien-Behandlungsstandard beim fortgeschrittenen RCC wird.
Choueiri T et al., ESMO 2020, Abstract #696O_PR
Die Behandlung mit Immun-Checkpoint-Inhibitoren bringt relevante Vorteile für Patienten mit Magen- und Ösophaguskarzinomen, die derzeit eine schlechte Prognose haben. Das zeigen gleich drei beim ESMO-Kongress präsentierte Studien, die als praxisverändernd gelten. Derzeit sind Checkpoint-Inhibitoren in westlichen Ländern beim Magen- und Ösophaguskarzinom noch nicht für eine Therapie in frühen Linien zugelassen. Die aktuellen Studiendaten vom ESMO legen jedoch nahe, dass sich das bald ändern dürfte.
In der Phase-III-Studie CheckMate-649 wurde der PD-1-Inhibitor Nivolumab zusammen mit Chemotherapie im Vergleich zur Chemotherapie alleine als Erstlinientherapie bei Patienten mit HER-2-negativem, fortgeschrittenem Magenkarzinom, Karzinomen des gastroösophagealen Übergangs und Ösophaguskarzinom – alle mit Adenokarzinom-Histologie – evaluiert. Die Ergebnisse zeigen, dass Nivolumab und Chemotherapie das Gesamtüberleben (OS) und progressionsfreie Überleben (PFS) bei Patienten mit PD-L1-positiven Tumoren (Combined Positive Score [CPS] ≥ 5) gegenüber alleiniger Chemotherapie verbesserten (medianes OS 14,4 vs. 11,1 Monate; HR 0,71; p < 0,0001; medianes PFS 7,7 vs. 6,1 Monate; HR 0,68; p < 0,0001).[1] Verbesserungen wurden auch bei Tumorpatienten mit CPS ≥ 1 und in der gesamten Patientenpopulation beobachtet.
Die Phase-II-Studie ATTRACTION 4 ähnelte CheckMate-649, abgesehen davon, dass sie nur bei asiatischen Patienten (n = 40) durchgeführt wurde und keine speziellen Grenzwerte für den PD-L1-Status festgelegt waren. Die Erstlinientherapie mit Nivolumab plus Chemotherapie verbesserte den koprimären Endpunkt PFS auf klinisch relevante Weise (medianes PFS 10,5 vs. 8,3 Monate; HR 0,68; p = 0,0007), verfehlte aber eine signifikante Verbesserung des OS (HR 0,90).[2] In der Phase-III-Studie KEYNOTE-590 wurde schließlich der PD-1-Inhibitor Pembrolizumab zusammen mit Standard-Chemotherapie gegenüber Chemotherapie alleine im Erstliniensetting bei 749 Patienten mit lokal fortgeschrittenem/unresezierbarem oder metastasierendem Adenokarzinom, Plattenepithelkarzinom des Ösophagus oder Siewert-Typ-I-Adenokarzinom des ösophagogastralen Übergangs evaluiert. Koprimäre Endpunkte waren das OS und PFS.
Wie Dr. Ken Kato, Tokio, Japan, berichtete, führte die Kombination Pembrolizumab/Chemotherapie im Vergleich zur Chemotherapie alleine zu einer statistisch signifikanten und klinisch relevanten Verbesserung aller klinischen Wirksamkeitsparameter – OS (median 12,4 vs. 9,8 Monate; HR 0,73; p < 0,0001) und PFS (median 6,3 vs. 5,8 Monate; HR 0,65; p < 0,0001) sowie Gesamtansprechrate (ORR; 45,0 % vs. 29,3 %).[3]
1 Moehler M et al., ESMO 2020, Abstract LBA6_PR
2 Boku N et al., ESMO 2020, Abstract LBA7_PR
3 Kato K et al., ESMO 2020, Abstract LBA8_PR
Bildnachweis: from2015 (iStockphoto)