
Während Estron, Estradiol und Estriol bereits in den 1930er-Jahren entdeckt wurden, kam man Estetrol erst viel später auf die Spur. Und schnell verschwand es wieder in der Versenkung. Erst in den vergangenen 25 Jahren hat man seine ganz speziellen Eigenschaften erkannt, die es für pharmakologische Anwendungen interessant machen.
Estetrol (E4) ist ein natürliches Estrogen, das 1965 von Egon Diczfalusy und Kollegen am Karolinska-Institut in Stockholm entdeckt wurde [1]. Es gehört zur Familie der natürlichen Estrogene, zu der auch Estron (E1), Estradiol (E2) und Estriol (E3) zählen [2]. Strukturell zeichnet sich E4 durch das Vorhandensein von 4 Hydroxylgruppen aus, was es von den anderen Estrogenen unterscheidet. E4 wird nahezu ausschließlich in der fetalen Leber des Menschen synthetisiert und ist ab der 9. Schwangerschaftswoche im mütterlichen Urin nachweisbar. Die Konzentrationen von unkonjugiertem E4 im mütterlichen Plasma steigen im Verlauf der Schwangerschaft stetig an und erreichen gegen Ende der Schwangerschaft Werte von mindestens 1 ng/ml. Diese peripartale Maximierung könnte ein Hinweis auf eine Schutzfunktion vor hypoxischen Noxen im Rahmen der Geburt sein, wie einschlägige Tierversuche durch die E4-vermittelte Gewebeprotektion ausweisen. Im fetalen Plasma werden zum Zeitpunkt der Geburt mehr als 10-fach höhere Konzentrationen als im mütterlichen Plasma gemessen [2]. Obwohl die physiologische Funktion von E4 während der Schwangerschaft letztlich bislang unbewiesen ist, legt die natürliche Exposition gegenüber relativ hohen E4-Konzentrationen eine gute Verträglichkeit des (Wirk-)Stoffs nahe. Möglicherweise schützt E4 den Feten (und vielleicht auch die Mutter) vor den hochpotenten Steroiden in der Schwangerschaft – das wäre eine biologisch plausible Erklärung.
Pharmakologie
Die einzigartige Struktur mit 4 Hydroxylgruppen verleiht E4 besondere pharmakologische Eigenschaften [3,4]:
E4 zeichnet sich durch eine schnelle Absorption nach oraler Gabe mit maximalen Plasmakonzentrationen nach 0,5–2 Stunden und eine lange Halbwertszeit von 28–32 Stunden aus. E4 ist ein Endprodukt des Steroidmetabolismus und wird nicht in Estron, Estronsulfat, Estradiol oder Estriol umgewandelt. E4 wird nicht über Cytochrom P450-Enzyme metabolisiert und inhibiert diese folglich nicht [3,4]. E4 hat eine agonistische Wirkung am nukleären Estrogenrezeptor α (ERα) und eine antagonistische am membranständigen ERα sowie eine höhere Affinität für ERα im Vergleich zu ERβ. Im Gegensatz zu klassischen selektiven Estrogenrezeptor-Modulatoren (SERMs) wie Tamoxifen oder Raloxifen interagiert E4 mit der Ligandenbindungsdomäne des ERα, ähnlich wie die anderen natürlichen Estrogene, und rekrutiert dieselben Co-Regulatoren. Die unterschiedlich verteilten Rezeptormuster gemeinsam mit der exklusiven E4-spezifischen Antagonisierung des membranständigen ERα sorgen für das einzigartige, weil organspezifische Wirkprofil. E4 wird daher als einzige Substanz der Wirkstoffklasse der NESTs (Native Estrogen with Selective action in Tissues) zugeordnet.
Im Gegensatz zu allen anderen Estrogenen weist Estetrol keine Bindung an SHBG auf.
Im Vergleich zu E2 hat E4 eine relativ geringe Affinität zum Estrogenrezeptor. E4 besitzt etwa 6 % der Affinität von Estradiol. Daraus resultiert eine Wirksamkeit von 2–3 % vs. E2. Es ist also ein relativ schwach wirksames Estrogen. Unter anderem deswegen hat man die Estetrol-Forschung in den 1980er-Jahren auch weitgehend eingestellt. Man wusste mit der schwach wirksamen Substanz nicht viel anzufangen, übersah aber den damit verbundenen Vorteil reduzierter estrogenbedingter Nachteile. E4 besitzt eine hohe Spezifität für ERα und bindet dort mit 5-fach höherer Affinität als ERβ an. Damit wird dosisabhängig E2 vom (proliferativen) ERα verdrängt und kann sekundär an den (protektiven) ERβ binden [3,4]. Was verwirrend klingt, hat eine biologische Rationale. Der (proliferative) ERα wird durch das dort mit viel höherer Affinität bindende E4 blockiert und aufgrund dessen im Vergleich zu E2 viel schwächeren Wirkung kaum stimuliert, während der (protektive) ERβ für die Bindung von E2 zur Verfügung steht, das dort an den jeweiligen kritischen Geweben seine entsprechende Wirkung zur Entfaltung bringen kann.
Physiologie
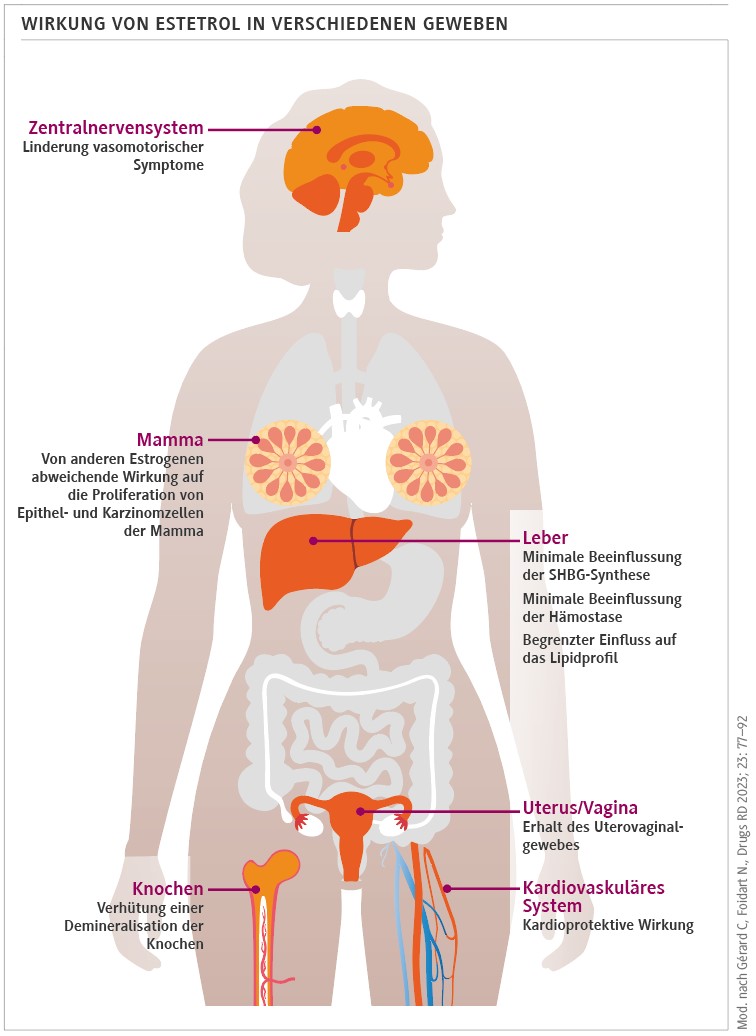
Diese selektive Rezeptoraktivierung führt zu unterschiedlichen Wirkungen in verschiedenen Geweben (Abb.) [3-5]:
E4 zeigt neuroprotektive Effekte im zentralen Nervensystem. Studien an ovarektomierten Ratten haben gezeigt, dass E4 die Expression von Allopregnanolon und β-Endorphin im Serum sowie in verschiedenen Hirnarealen wie dem frontalen Kortex, dem Hippocampus und der Hypophyse erhöht. Diese Wirkung könnte zur Linderung von Wechseljahresbeschwerden beitragen. E4 hat zudem potente antigonadotrope Effekte, indem es die Sekretion von luteinisierendem Hormon (LH) und follikelstimulierendem Hormon (FSH) unterdrückt [6]. E4 zeigt vaskuloprotektive Eigenschaften, die zur Prävention von Atherosklerose beitragen können. Es fördert die Produktion von Stickstoffmonoxid in Endothelzellen, was zu einer Vasodilatation führt. Darüber hinaus verhindert E4 die Entwicklung von Hypertonie und reduziert die alters- und hypertensionsbedingte arterielle Versteifung [7]. E4 hat positive Auswirkungen auf den Knochenstoffwechsel. Es erhöht die Knochenmineraldichte und verbessert die Mineralisierung der Wirbelkörper. Zudem stärkt es den Knochen gegen biomechanische Schäden und beeinflusst den Serumosteocalcinspiegel. In klinischen Studien wurde eine signifikante Abnahme des Knochenabbaumarkers CTX-1 bei postmenopausalen Frauen beobachtet, die mit E4 behandelt wurden [8].
Estetrol hat positive Auswirkungen auf den Knochenstoffwechsel.
Im Brustdrüsengewebe hat E4 eine äußerst schwache estrogene Wirkung und kann in Gegenwart von Estradiol sogar antiestrogen wirken. In-vitro- und In-vivo-Studien haben gezeigt, dass E4 im Vergleich zu Estradiol eine 100-fach geringere Potenz bei der Stimulierung der Proliferation von Brustepithelzellen aufweist. Im Brustdrüsengewebe hat E4 also eine äußerst schwache estrogene Wirkung und kann in Gegenwart von Estradiol sogar antiestrogen wirken [9]. Diese Eigenschaft könnte E4 zu einer interessanten Option für die Behandlung von Brustkrebs machen. E4 wirkt als typischer Estrogenagonist im Endometrium und im Uterus. Es stimuliert das Wachstum des Uterus und die epitheliale Proliferation [10]. Bei postmenopausalen Frauen führt die Behandlung mit E4 zu einer dosisabhängigen Zunahme der Endometriumdicke, ohne jedoch Endometriumhyperplasien zu verursachen. E4 zeigt auch deutliche estrogene Effekte am Vaginalepithel. Es verbessert die vaginale Zytologie, indem es den Anteil an Superfizialzellen erhöht und den Anteil an Parabasal- und Intermediärzellen verringert. Zudem senkt E4 den vaginalen pH-Wert und lindert Symptome des genitourinären Syndroms der Menopause wie vaginale Trockenheit und Dyspareunie [10].
Diese vielfältigen physiologischen Effekte machen E4 zu einem vielversprechenden Wirkstoff für verschiedene gynäkologische Anwendungen, insbesondere in der Hormonersatztherapie und als Komponente in oralen Kontrazeptiva. Seine selektive Wirkung in verschiedenen Geweben trägt zu einem günstigen Nutzen-Risiko-Profil bei. E4 scheint im Vergleich zu anderen Estrogenen geringere Auswirkungen auf die Hämostase zu haben. In einer Studie mit postmenopausalen Frauen zeigte sich kein signifikanter Einfluss auf Gerinnungsparameter. Dies könnte auf ein potenziell geringeres Risiko für venöse Thromboembolien (VTE) hindeuten. Auch die Auswirkungen von E4 auf den Stoffwechsel scheinen minimal zu sein. Studien zeigten keine klinisch relevanten Veränderungen von Lipidprofil, Glucosehomöostase oder Leberenzymwerten.

In den vergangenen Jahren wurde E4 intensiv erforscht, insbesondere im Hinblick auf seine Anwendung als Estrogen-Komponente in kombinierten oralen Kontrazeptiva und als mögliche Behandlungsoption für menopausale Symptome. Die präklinischen und klinischen Daten deuten auf eine gewebespezifische Aktivität und ein selektiveres pharmakologisches Profil im Vergleich zu anderen Estrogenen hin, einschließlich einer geringen Auswirkung auf die Leber und die Hämostase. Diese pharmakologischen Eigenschaften tragen zu seinem günstigen Nutzen-Risiko-Profil bei und machen Estetrol zu einer vielversprechenden Option für verschiedene klinische Anwendungen in der Gynäkologie und möglicherweise weit darüber hinaus.

Der Autor

Dr. med. Ludwig N. Baumgartner
Facharzt für Frauenheilkunde und Geburtshilfe
Marienplatz 3, 85354 Freising
Bildnachweis: grebeshkovmaxim, Pikovit44 (gettyimages); privat